Από τον Mad Scientist.
Γνωρίζοντας το μινιμαλιστικό στυλ των αιθουσών διδασκαλίας στα ελληνικά σχολεία μπορώ να πω με σχετική βεβαιότητα ότι το μόνο που υπάρχει μέσα στη τάξη είναι ένας περιοδικός πίνακας. Αν όχι…κάντε κατάληψη!
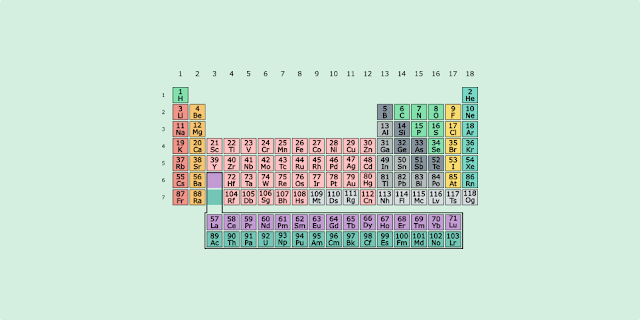
Τι είναι όμως αυτός ο περίεργος πίνακας με τα ακαταλαβίστικα γράμματα και τα σκόρπια νούμερα; Πρόκειται για τον περιοδικό πίνακα των στοιχείων για τον οποίο έχει μείνει γνωστός ο Ρώσος χημικός Dimitri Mendeleyev (αν και δεν ήταν ο μόνος που έφτιαξε ένα τέτοιο πίνακα) και είναι ένα μοναδικό παράδειγμα της δύναμης πρόβλεψης που μας δίνει η επιστημονική μεθοδολογία. Όχι πρόβλεψης του στυλ “είσαι Ζυγός” άρα πρόσεξε γιατί κάποιος μέσα στον μήνα θα σε βρίσει στον δρόμο, αλλά του στυλ “αυτός ο κομήτης θα περάσει κοντά από τη Γη στην τάδε πλευρά εκείνη τη μέρα” (βλέπε κομήτης Halley). Όπως εξήγησε και ο Στέφανος στο βίντεό του σχετικά με την επιστημονική μέθοδο, ο τρόπος με τον οποίο εξετάζουμε τη φυσική πραγματικότητα στο πλαίσιο μιας επιστημονικής έρευνας μας δίνει τη δυνατότητα να προβλέψουμε τα πιθανά αποτελέσματα μια δεδομένης πράξης ή φαινομένου. Για παράδειγμα, αν ρίξουμε ένα αμόνι από τον πύργο του Άιφελ (όχι ότι θα σας άφηναν να περάσετε αμόνι από τον έλεγχο αλλά λέμε τώρα!), γνωρίζοντας τις συνθήκες του περιβάλλοντος και το βάρος του αντικειμένου μπορούμε να προβλέψουμε με μεγάλη ακρίβεια πόση ώρα θα χρειαστεί για να πέσει στο έδαφος και που ακριβώς θα πέσει.
Ωστόσο, ενώ σήμερα γνωρίζουμε αρκετά για την ύλη και τις αλληλεπιδράσεις της, αυτό δεν ίσχυε πριν μερικές εκατοντάδες χρόνια. Για παράδειγμα, η χημεία που γνωρίζουμε σήμερα δεν υπήρχε με αυτή τη μορφή το 1500. Υπήρχε στη πρώιμη μορφή της, την αλχημεία. Οι αλχημιστές ήταν άνθρωποι οι οποίοι είχαν συνήθως μεγάλη περιουσία και επιδίδονταν σε περίπλοκα και επικίνδυνα πειράματα με σκοπό τη μετατροπή κοινών υλικών σε χρυσό και τη παραγωγή του ελιξηρίου της αθανασίας. Μέσα από τα πειράματα τους, από πολλά λάθη, δοκιμές και ακρωτηριασμούς (πολλούς ακρωτηριασμούς…) αναδύθηκαν πρακτικές που αργότερα αποτέλεσαν τον ακρογωνιαίο λίθο της σημερινής χημείας.
Από τη δουλειά των αλχημιστών λοιπόν και από μεταγενέστερες διορθώσεις και ανακαλύψεις που έγιναν στο πλαίσιο της συμβατικής, πλέον, χημείας μπορέσαμε να ορίσουμε τα δομικά χαρακτηριστικά της ύλης με χαρακτηριστικό παράδειγμα το χημικό στοιχείο. Χημικό στοιχείο είναι μια τάξη ατόμων με καθορισμένο αριθμό πρωτονίων στο πυρήνα τους, όπως για παράδειγμα τα άτομα Υδρογόνου. Πιο αναλυτικά, ένα άτομο αποτελείται από τον πυρήνα, ο οποίος συγκροτείται από πρωτόνια και νετρόνια και ένα νέφος ηλεκτρονίων τα οποία κινούνται γύρω από τον πυρήνα.
Φανταστείτε το σαν ένα ποδοσφαιρικό στάδιο όπου στο κέντρο είναι ο πυρήνας και σε κάθε επίπεδο θέσεων στις κερκίδες βρίσκονται ηλεκτρόνια. Η πραγματικότητα φυσικά είναι λίγο πιο περίπλοκη, καθώς δεν έχουμε συγκεκριμένο χώρο στον οποίο κινούνται τα ηλεκτρόνια αλλά περιοχές γύρω από τον πυρήνα όπου υπάρχει μεγαλύτερη πιθανότητα να βρίσκονται τα ηλεκτρόνια. Πολύ χοντρικά, τα ηλεκτρόνια είναι σαν τα πεντάχρονα, μπορείς να ξέρεις μόνο τους πιθανούς χώρους στους οποίους θα βρεθούν το επόμενο δευτερόλεπτο όχι ακριβή θέση και προσανατολισμό.
Σε ένα στοιχείο τα ηλεκτρόνια είναι ισάριθμα με τα πρωτόνια με αποτέλεσμα να υπάρχει ηλεκτρική ουδετερότητα καθώς τα πρωτόνια είναι θετικά φορτισμένα και τα ηλεκτρόνια αρνητικά φορτισμένα, έτσι το άθροισμα των φορτίων βγαίνει μηδέν.
Χημικό μόριο είναι δυο άτομα από τα ίδια ή διαφορετικά στοιχεία τα οποία ενώνονται μεταξύ τους. Για παράδειγμα δυο άτομα οξυγόνου ενωμένα μεταξύ τους είναι ένα μόριο οξυγόνου όπως και ένα άτομο υδρογόνου, ένα άτομο άνθρακα και ένα άτομο αζώτου ενωμένα μεταξύ τους αποτελούν ένα μόριο υδροκυανίου το οποίο τους τελευταίους μήνες σκέφτομαι σοβαρά να συνθέσω για προσωπική χρήση.
Ο περιοδικός πίνακας είναι ένας χάρτης στον οποίο έχουμε ταξινομήσει τα μέχρι τώρα γνωστά χημικά στοιχεία με βάση κάποια χαρακτηριστικά τους, όπως για παράδειγμα το ατομικό τους βάρος, το τρόπο με τον οποίο κατανέμονται τα ηλεκτρόνια τους γύρω από τον πυρήνα καθώς και τις χημικές τους ιδιότητες. Οκ, θα πει κάποιος, και λοιπόν; Βάλατε τα στοιχεία σε σειρά, συγχαρητήρια! Δεν είναι κάποιο επίτευγμα! Μμμμμ, για όποιον έχει αυτή την άποψη, θα σας απογοητεύσω. Η ταξινόμηση των στοιχείων στο περιοδικό πίνακα πέρα από του ότι μας έδωσε τη δυνατότητα να μπορούμε να προβλέψουμε με ακρίβεια τις ιδιότητες ενός στοιχείου από τα στοιχεία που βρίσκονται γύρω του και κατά συνέπεια τη δυνατότητα να γνωρίζουμε τις ιδιότητες στοιχείων που δεν έχουμε ανακαλύψει ακόμα, μας επιτρέπει να σχεδιάζουμε νέες ενώσεις αξιοποιώντας τις πληροφορίες που αντλούμε από τις ιδιότητες των στοιχείων. Ωστόσο θεωρώ πιο εντυπωσιακή τη πορεία που διένυσε η σύγχρονη χημεία από τις αρχαίες αντιλήψεις περί ύλης μέχρι το σημείο όπου πουλούσαμε πλέον μούρη και προβλέπαμε τη σύνθεση άγνωστων στοιχείων.
Η προσπάθεια να ταξινομήσουμε τα χημικά στοιχεία δεν ήταν καινούργια ιδέα ακόμα και στην εποχή του Mendeleyev. Πολλοί μεγάλοι επιστήμονες είχαν προσπαθήσει να βρουν ένα σύστημα οργάνωσης των στοιχείων με βάση διαφορετικά χαρακτηριστικά έτσι ώστε να μπορούν να βρουν τι συνδέει διαφορετικά χημικά στοιχεία μεταξύ τους. Κρατήστε στο νου σας ότι εκείνη την εποχή δεν είχαμε τα ίδια εργαλεία που έχουμε σήμερα, δεν είχαμε ανακαλύψει ούτε τα μισά από τα χημικά στοιχεία που υπάρχουν αυτή τη στιγμή στον περιοδικό πίνακα.
Μια από τις πρώτες σοβαρές προσπάθειες οργάνωσης των χημικών στοιχείων έγινε από τον Antoine Lavoisier ο οποίος ταξινόμησε τα 33 στοιχεία τα οποία ήταν γνωστά εκείνη την εποχή στις κατηγορίες: “αέρια”, “μέταλλα”, “αμέταλλα” και “γαίες”.
Ο περιοδικός πίνακας του Antoine Lavoisier
Ένας άλλος χημικός, ο Γερμανός Johann Wolfgang Döbereiner αποφάσισε να ταξινομήσει τα στοιχεία με βάση τις χημικές τους ιδιότητες. Προσπαθούσε να δει ποια στοιχεία αντιδρούσαν με τον ίδιο ή παραπλήσιο τρόπο σε συγκεκριμένες χημικές αντιδράσεις και με βάση αυτό τα ταξινομούσε σε ομάδες. Άλλες προσεγγίσεις ήταν η οργάνωση των στοιχείων με βάση τα ατομικά τους βάρη δηλαδή πολύ, πολύ χοντρικά, πόσο πιο “βαρύ” είναι ένα στοιχείο σε σχέση με το άτομο του υδρογόνου που χρησιμοποιείται ως σημείο αναφοράς. Και αυτή τη δουλειά έκαναν χημικοί όπως ο Jöns Jacob Berzelius ο οποίος μάλιστα θέλοντας να παράγει ακριβή αποτελέσματα και δεδομένου ότι τα όργανα μέτρησης της εποχής προφανώς δε κάλυπταν τις ανάγκες του, αποφάσισε να φτιάξει ο ίδιος τον εξοπλισμό του. Με λίγα λόγια πήγε την έννοια αποφασιστικότητα σε άλλο επίπεδο!
Μία από τις συνεισφορές του Berzelius στη χημεία, πέρα από την ταυτοποίηση του πυριτίου, του σεληνίου, του θορίου και του δημητρίου φυσικά, ήταν το σύστημα γραφής των χημικών στοιχείων που χρησιμοποιούσε για ευκολία στα πειράματα του και το οποίο συνεχίζουμε να χρησιμοποιούμε ακόμα και σήμερα. Τα σύμβολα Fe για το σίδηρο και O για το οξυγόνο, για παράδειγμα, είναι επινόηση του Berzelius.
Άλλη σημαίνουσα μορφή στη προσπάθεια ταξινόμησης των χημικών στοιχείων ήταν ο John Newlands ο οποίος ανακάλυψε κάτι πολύ ενδιαφέρον ερευνώντας τα ατομικά βάρη των στοιχείων. Παρατήρησε πως όταν τα χημικά στοιχεία οργανώνονταν με σειρά αυξανόμενου ατομικού βάρους, εμφανίζονταν παρόμοιες φυσικές και χημικές ιδιότητες ανά 8 στοιχεία, φαινόμενο που ονόμασε νόμο της οκτάβας (από τις οκτάβες σε ένα πιάνο).
Αυτό το φαινόμενο όπως διαπιστώσαμε πολλά χρόνια μετά οφείλονταν στον τρόπο με τον οποίο κατανέμονται τα ηλεκτρόνια στο κάθε στοιχείο που με τη σειρά του ορίζει την ικανότητα της εκάστοτε ένωσης να συμμετέχει σε συγκεκριμένες αντιδράσεις και να εμφανίζει τις αντίστοιχες χημικές ιδιότητες, όπως για παράδειγμα να αναφλέγεται στον αέρα όπως συμβαίνει με τον λευκό φώσφορο.
Βλέπουμε λοιπόν ότι η ταξινόμηση δεν ήταν απλώς προσπάθεια οργάνωσης αυτών που γνωρίζαμε ήδη για τα χημικά στοιχεία αλλά και τρόπος να μάθουμε περισσότερα γι’ αυτά μέσω συσχετισμού των ιδιοτήτων τους και παρότι η υπόθεση του Newlands αντιμετωπίστηκε με χλεύη από τους συγχρόνους του αρχικά, άλλοι επιστήμονες αξιοποίησαν το έργο του και έχτισαν πάνω σε αυτή τη βάση επεκτείνοντας τις γνώσεις μας πάνω στις ιδιότητες των χημικών στοιχείων.
Και κάπου εδώ έρχεται στο προσκήνιο ο Mendeleev. Ως νέος φοιτητής ο Mendeleev είχε την τύχη να παρακολουθήσει το πρώτο παγκόσμιο συνέδριο χημείας στο οποίο βασικό θέμα ήταν η προσπάθεια διαλεύκανσης του μυστηρίου των ατομικών βαρών. Για να μη μπούμε σε πολλές ιστορικές λεπτομέρειες ας κρατήσουμε απλά στο μυαλό μας ότι αυτό το συνέδριο έδωσε στον Mendeleev την κατάλληλη ώθηση προκειμένου να παθιαστεί με την ταξινόμηση των χημικών στοιχείων και την ανακάλυψη των ιδιοτήτων που τα συνδέουν μεταξύ τους.
Ο Mendeleyev λοιπόν στη προσπάθεια του να βρει αυτή τη σύνδεση, και παράλληλα για να κάνει τη διδασκαλία των χημικών στοιχείων πιο απλή και ευχάριστη για τους φοιτητές του, χρησιμοποίησε μικρές κάρτες και έγραψε σε κάθε μια από ένα χημικό στοιχείο και το ατομικό του βάρος. Μέχρι τότε η ταξινόμηση των στοιχείων είχε γίνει είτε με βάση το ατομικό βάρος είτε μέσω των χημικών ιδιοτήτων. Η ιδέα του Mendeleyev λοιπόν ήταν να συνδυάσει αυτά τα δυο. Ωστόσο για να βγάζει νόημα ο πίνακας με βάσει τα γνωστά στοιχεία που υπήρχαν μέχρι τότε και τα οποία είχε διαθέσιμα, έπρεπε να κάνει κάτι περίεργο, έπρεπε να αφήσει κενά.
Το μοντέλο ταξινόμησης που εφηύρε λοιπόν του επέτρεψε να κάνει κάτι που μόνο στο πεδίο της επιστήμης έχει τεκμηριωθεί ως πραγματική ικανότητα, του επέτρεψε να προβλέψει το μέλλον.
Στην πρώτη έντυπη έκδοση του περιοδικού πίνακα βλέπουμε συμπληρωμένα ατομικά βάρη με κενά τα στοιχεία, που σημαίνει ότι ο Mendeleyev ήξερε πως, προκειμένου το μοντέλο του να είναι σωστό έπρεπε να υπάρχουν χημικά στοιχεία με τα ατομικά βάρη που σημείωσε, τα οποία όμως δεν είχαν βρεθεί ακόμα. Και το πιο εξωφρενικό είναι ότι εκτός από τα ατομικά βάρη, προέβλεψε με μεγάλη ακρίβεια και τις χημικές ιδιότητες που θα είχαν αυτά τα στοιχεία με βάση τη θέση τους στον πίνακα, δηλαδή με βάση το ποια στοιχεία τα περιέβαλλαν.
Δεδομένου λοιπόν ότι το poster του περιοδικού πίνακα υπάρχει σήμερα σε κάθε εργαστήριο χημείας στο κόσμο, όπως καταλαβαίνετε ο κύριος με το περίεργο μούσι είχε δίκιο τελικά. Όχι σε όλα φυσικά, έκανε ορισμένα λάθη στα ατομικά βάρη κάποιων στοιχείων αλλά το γενικό concept ήταν σωστό.
Σήμερα έχουμε 118 γνωστά χημικά στοιχεία, 94 εκ των οποίων μπορούν να προκύψουν στο περιβάλλον χωρίς ανθρώπινη παρέμβαση, αν και τα περισσότερα λόγω δραστικότητας βρίσκονται με τη μορφή διάφορων ενώσεων, ενώ τα υπόλοιπα 24 έχουν συντεθεί μόνο σε εργαστηριακό πλαίσιο. Αυτή τη στιγμή μάλιστα διεξάγονται πειράματα τα οποία εξετάζουν τη πιθανότητα σύνθεσης χημικών στοιχείων με μεγαλύτερα ατομικά βάρη από τα γνωστά.
Ποιο είναι το συμπέρασμα από όλα αυτά; Δεν υπάρχουν μικρές και μεγάλες συνεισφορές στην επιστήμη. Κάθε ανακάλυψη, κάθε έρευνα, κάθε στοιχείο που συνεισφέρει ένας ερευνητής στη διεθνή επιστημονική κοινότητα είναι μια εν δυνάμει ώθηση στον επόμενο ή στους επόμενους Mendeleyev. Η επόμενη μεγάλη ανακάλυψη μπορεί αν έρθει από κάποιον που διαβάζει αυτές τις γραμμές και αυτός ή αυτή με τη σειρά τους θα δώσουν το έναυσμα στην επόμενη γενιά να συνεχίσει την έρευνα του φυσικού κόσμου. Αυτή είναι η ομορφιά της επιστήμης, ότι όσοι ασχολούμαστε με αυτή βρισκόμαστε με το ένα πόδι στην ασφάλεια της γνώσης και με το άλλο στην εθιστική αίσθηση της άγνοιας παίζοντας ένα συνεχές παιχνίδι σκυταλοδρομίας μεταξύ γενεών. Όπως έχει πει πολλάκις και ο Neil deGrasse Tyson, δε μπορείς να είσαι επιστήμονας αν έχεις πρόβλημα με την άγνοια. Πάντα υπάρχουν και θα υπάρχουν πράγματα που δε γνωρίζουμε. Ωστόσο, όπως ο Mendeleev οφείλουμε να βάλουμε τα στοιχεία κάτω και να αφήσουμε αυτά να μας οδηγήσουν.
Δείτε το σχετικό βίντεο
Περισσότερες πληροφορίες
http://goldbook.iupac.org/html/C/C01022.html (Ορισμός της έννοιας "χημικό στοιχείο")
http://www.rsc.org/education/teachers/resources/periodictable/pre16/develop/mendeleev.htm (Η μέθοδος των καρτών με τα χημικά στοιχεία από τον Mendeleev)
https://www.chemheritage.org/historical-profile/j%C3%B6ns-jakob-berzelius (Η επινόηση των χημικών συμβολισμών από τον Bezelius)
https://www.dropbox.com/s/92wqj7mazv2sn5n/From%20Triads%20to%20Catalysis%20Johann%20Wolfgang%20D%C3%B6bereiner%20%281780%E2%80%931849%29%20on%20the%20150th%20Anniversary%20of%20His%20Death.pdf?dl=0 (Ο νόμος της τριάδας του Dobereiner)
https://www.acs.org/content/acs/en/education/whatischemistry/landmarks/lavoisier.html#new-chemistry-emerges (Έρευνα σχετικά με περιπτώσεις όπου επιγεννετικές αλλαγές ξεφεύγουν από τους επιδιορθωτικούς μηχανισμούς του οργανισμού)
https://www.dropbox.com/s/1gpbpr3o2hljp9y/The%20history%20of%20chemical%20laboratory%20equipment.pdf?dl=0 (Εξέλιξη του εργαστηριακού εξοπλισμού)
https://www.chemistryworld.com/news/beyond-element-118-the-next-row-of-the-periodic-table/9400.article (Προσπάθεια για επέκταση του περιοδικού πίνακα πέρα από τα γνωστά χημικά στοιχεία)